Pruebas en el diagnóstico y progresión
EN ESTE ARTÍCULO

Mutaciones sensibilizantes y de resistencia al EGFR
Las mutaciones sensibilizantes del receptor del factor de crecimiento epidérmico (EGFR) están presentes en los tumores de aproximadamente 30 a 47% de los pacientes asiáticos y de 10 a 22% de los pacientes occidentales con cáncer de pulmón de células no pequeñas (NSCLC).1–9
Se recomienda que a todos los pacientes con NSCLC avanzado e histología de adenocarcinoma se les realicen pruebas de mutaciones de EGFR.9–13 Sin embargo, no se recomienda la prueba de mutaciones de EGFR para pacientes con un diagnóstico seguro de carcinoma de células escamosas que carece de cualquier componente de adenocarcinoma, excepto bajo la luz de nunca/antes. fumadores (<15 paquetes año).9–11
El estado de mutación del EGFR tumoral de un paciente puede determinarse realizando una prueba de mutación del EGFR de diagnóstico para buscar la presencia o ausencia de mutaciones en el ADN del tumor que codifica el gen del EGFR. La prueba de mutación de EGFR debe ser sólida, confiable, de alta calidad y realizarse en el menor tiempo posible, con una práctica de diagnóstico estándar bien validada y alineada.
Para los pacientes con diagnóstico de NSCLC avanzado que albergan una mutación activadora o sensibilizante del EGFR, el estándar de atención es el tratamiento de primera línea con un inhibidor de la tirosina quinasa del EGFR (EGFR-TKI), como afatinib, erlotinib o gefitinib.9,11 Las mutaciones activadoras más comunes antes del tratamiento con un EGFR-TKI se observaron deleciones en el exón 19 y una mutación puntual L858R en el exón 21.14–17
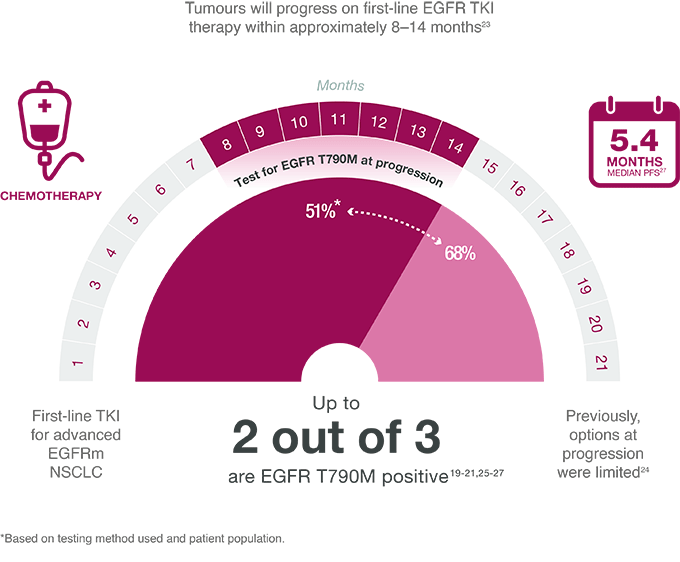
A pesar de las altas tasas de respuesta inicial a los EGFR-TKI de primera línea, la mayoría de los pacientes con NSCLC avanzado que albergan una mutación de EGFR progresarán con el tratamiento debido a la resistencia adquirida, con una mediana de supervivencia libre de progresión de 9,7 a 13,1 meses.18,19
Las pruebas de mutación en la progresión de la enfermedad se pueden utilizar para ayudar a identificar los mecanismos de resistencia adquirida. El mecanismo más común de resistencia adquirida es la mutación EGFR T790M.20-23
Pruebas en el diagnóstico y progresión
Pruebas en el diagnóstico
Aproximadamente el 90 % de las mutaciones de EGFR son deleciones en el exón 19 o mutaciones puntuales L858R en el exón 21,15,28 para las cuales existen extensos datos de ensayos clínicos aleatorizados que respaldan la sensibilidad de los tumores que albergan estas mutaciones al tratamiento con EGFR-TKI.4,5,15-17,29-31
En el diagnóstico primario de NSCLC avanzado, los resultados de la prueba de mutación de EGFR ayudan a los médicos a decidir si es probable que un paciente se beneficie del tratamiento con un EGFR-TKI. Por lo tanto, los resultados de la prueba de mutación de EGFR deben informarse claramente e incluir el tipo de mutación para permitir que el médico tome una decisión de tratamiento basada en la evidencia disponible.
Al realizar pruebas para mutaciones de EGFR, se recomienda utilizar una muestra de tumor para confirmar la presencia de mutaciones de EGFR antes del tratamiento. Sin embargo, el ADN tumoral circulante (ctDNA) obtenido de la sangre (plasma) se puede utilizar si no se dispone de una muestra del tumor.32
El siguiente diagrama describe el proceso de análisis en el momento del diagnóstico utilizando muestras de tejido y plasma*.32
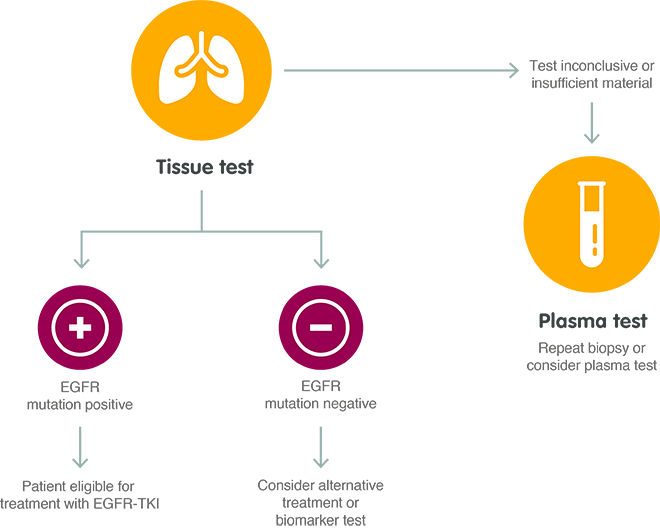
*Tenga en cuenta que las pruebas de mutación de EGFR con muestras de plasma no están aprobadas en Japón
Pruebas en la progresión
En la progresión de la enfermedad, los mecanismos de resistencia conocidos incluyen mutaciones adicionales de resistencia a EGFR (p. ej., T790M), activaciones de vías alternativas (p. ej., amplificación de HER2 o MET) o transformaciones fenotípicas (a cáncer de pulmón de células pequeñas [CPCP] o transición epitelial-mesenquimatosa).33,34
El mecanismo más común de resistencia adquirida a los EGFR-TKI de primera generación es la mutación EGFR T790M.20-23 Los estudios han demostrado que la incidencia de la mutación EGFR T790M en tumores que han desarrollado resistencia a los EGFR-TKI de primera generación varía de 51 al 68%.20–23,25
Por lo tanto, se recomienda enfáticamente que, en el momento de la progresión de la enfermedad, se realice una biopsia para confirmar la presencia de la mutación EGFR T790M y cualquier mutación conductora (p. ej., deleciones del exón 19 y mutaciones L858R) antes de continuar con el tratamiento.1,35,36
La prueba de la mutación T790M ahora es posible utilizando métodos similares a los de la prueba de mutación EGFR en el momento del diagnóstico primario. El estado de mutación de EGFR T790M se puede verificar mediante una prueba basada en tejido o en plasma.36
El siguiente diagrama describe el proceso de análisis en progresión utilizando plasma* y muestras tumorales.36
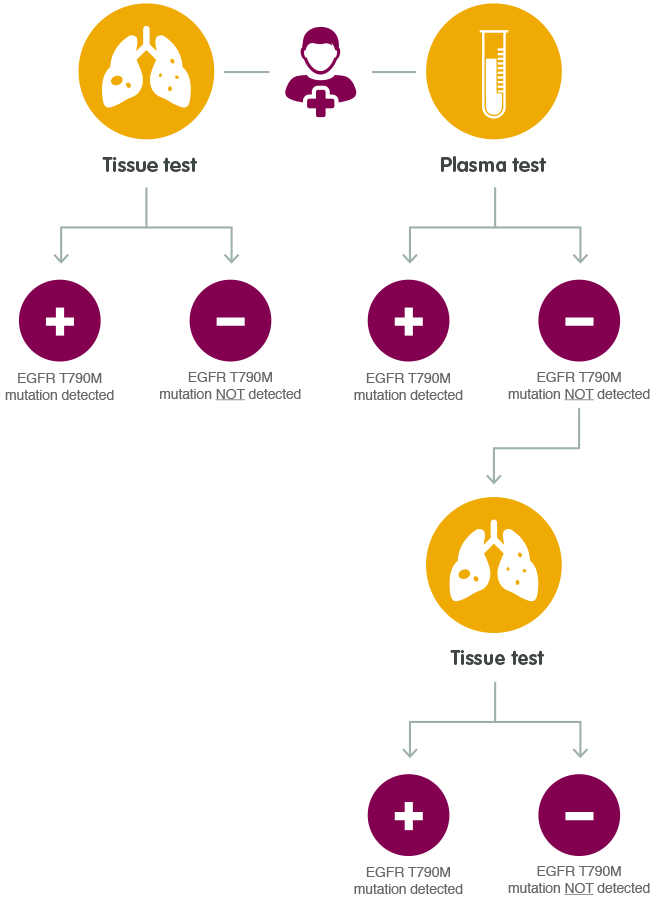
*Tenga en cuenta que las pruebas de mutación de EGFR con muestras de plasma no están aprobadas en Japón
Después de la progresión de la enfermedad, puede ser más difícil obtener una biopsia de tejido que en el diagnóstico primario. El ctDNA obtenido de una muestra de plasma ofrece una alternativa menos invasiva y potencialmente más rápida para la prueba de mutación de EGFR; sin embargo, la prueba de ctDNA es menos sensible para EGFR T790M que la deleción del exón 19 y L858R.37 Al usar la prueba de ctDNA, se debe tener en cuenta que los falsos negativos tienen (30-40%+).38,39 Por lo tanto, si se utiliza una prueba de ctDNA basada en plasma y el resultado es negativo, se recomienda que se haga un seguimiento con una prueba basada en tejido.36
Se recomienda encarecidamente una biopsia de tejido si el paciente está lo suficientemente bien como para tolerar el procedimiento, ya que esta es la fuente principal de las mutaciones. Al ordenar una prueba de ctDNA, se sugiere que también se solicite una biopsia de tejido, que se puede utilizar posteriormente si la prueba de ctDNA es negativa.
El panorama del tratamiento para pacientes con NSCLC avanzado y una mutación de EGFR está en constante evolución, con la disponibilidad del primer EGFR-TKI de tercera generación, osimertinib, que es un TKI irreversible selectivo oral que se dirige tanto a las mutaciones sensibilizantes de EGFR como específicamente al EGFR T790M. mutación conservando el EGFR de tipo salvaje.36
Referencias:
- Yang SH et al. Mutations in the tyrosine kinase domain of the epidermal growth factor receptor in non-small cell lung cancer. Clin Cancer Res 2005; 11: 2106–2110.
- Rosell R et al. Screening for epidermal growth factor receptor mutations in lung cancer. N Engl J Med 2009; 361: 958–967.
- Rosell R et al. Erlotinib versus standard chemotherapy as first-line treatment for European patients with advanced EGFR mutation-positive non-small-cell lung cancer (EURTAC): a multicentre, open-label, randomised Phase 3 trial. Lancet Oncol 2012; 13: 239–246.
- Douillard J-Y et al. First-line gefitinib in Caucasian EGFR mutation-positive NSCLC patients: a Phase-IV, open-label, single-arm study. Br J Cancer 2014; 110: 55–62.
- Han B et al. Determining the prevalence of EGFR mutations in Asian and Russian patients (pts) with advanced non-small-cell lung cancer (aNSCLC) of adenocarcinoma (ADC) and non-ADC histology: IGNITE study. Ann Oncol 2015; 26(suppl 1): i29–i44.
- Reck M et al. Investigating the utility of circulating-free tumour-derived DNA (ctDNA) in plasma for the detection of epidermal growth factor receptor (EGFR) mutation status in European and Japanese patients (pts) with advanced non-small-cell lung cancer (aNSCLC): ASSESS study. Ann Oncol 2015; 26(suppl 1): i57–i61.
- Schuette W et al. EGFR Mutation Status and First-line Treatment in Patients with Stage III/IV Non-small cell Lung Cancer in Germany: An Observational Study. Cancer Epidemiol Biomarkers Prev 2015; 24: 1254-1261.
- Midha A et al. EGFR mutation incidence in non-small-cell lung cancer of adenocarcinoma histology: a systematic review and global map by ethnicity (mutMapII). Am J Cancer Res 2015;5(9):2892-2911.
- Novello S et al. Metastatic non-small-cell lung cancer (NSCLC): ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2016; 27 (Suppl 5): v1-v27.
- Lindeman NI et al. Molecular testing guideline for selection of lung cancer patients for EGFR and ALK tyrosine kinase inhibitors: guideline from the College of American Pathologists, International Association for the Study of Lung Cancer, and Association for Molecular Pathology. Arch Pathol Lab Med 2013; 137: 828–860.
- NCCN. NCCN Clinical Practice Guidelines in Oncology NSCLC (version 4.2017), 2017. Available at: https://www.nccn.org/professionals/physician_gls/pdf/nscl.pdf. Accessed 25 January 2017.
- Keedy VL et al. American Society of Clinical Oncology provisional clinical opinion: epidermal growth factor receptor (EGFR) mutation testing for patients with advanced non-small-cell lung cancer considering first-line EGFR tyrosine kinase inhibitor therapy. J Clin Oncol 2011; 29: 2121–2127.
- Travis WD et al. International association for the study of lung cancer/american thoracic society/european respiratory society international multidisciplinary classification of lung adenocarcinoma. J Thorac Oncol 2011; 6: 244–285.
- Yoshida K et al. Prospective validation for prediction of gefitinib sensitivity by epidermal growth factor receptor gene mutation in patients with non-small cell lung cancer. J Thorac Oncol 2007; 2: 22–28.
- Mok TS et al. Gefitinib or carboplatin-paclitaxel in pulmonary adenocarcinoma. N Engl J Med 2009; 361: 947–957.
- Sequist LV et al. Phase III study of afatinib or cisplatin plus pemetrexed in patients with metastatic lung adenocarcinoma with EGFR mutations. J Clin Oncol 2013; 31: 3327–3334.
- Wu YL et al. Afatinib versus cisplatin plus gemcitabine for first-line treatment of Asian patients with advanced non-small-cell lung cancer harbouring EGFR mutations (LUX-Lung 6): an open-label, randomised phase 3 trial. Lancet Oncol 2014; 15: 213–222.
- Lee CK et al. Impact of specific epidermal growth factor receptor (EGFR) mutations and clinical characteristics on outcomes after treatment with EGFR tyrosine kinase inhibitors versus chemotherapy in EGFR-mutant lung cancer: a meta-analysis. J Clin Oncol 2015; 33: 1958–1965.
- Park K et al. Afatinib versus gefitinib as first-line treatment of patients with EGFR mutation-positive non-small-cell lung cancer (LUX-Lung 7): a phase 2B, open-label, randomised controlled trial. Lancet Oncol 2016 May;17(5): 577-89.
- Oxnard GR et al. Acquired resistance to EGFR tyrosine kinase inhibitors in EGFR-mutant lung cancer: distinct natural history of patients with tumours harboring the T790M mutation. Clin Cancer Res 2011; 17: 1616-1622.
- Sun JM et al. Clinical implications of T790M mutation in patients with acquired resistance to EGFR tyrosine kinase inhibitors. Lung Cancer 2013; 82: 294-298.
- Kuiper JL et al. Incidence of T790M mutation in (sequential) rebiopsies in EGFR-mutated NSCLC-patients. Lung Cancer 2014; 85: 19-24.
- Li W et al. T790M mutation is associated with better efficacy of treatment beyond progression with EGFR-TKI in advanced NSCLC patients. Lung Cancer 2014; 84: 295-300.
- Langer CJ. Epidermal growth factor receptor inhibition in mutation-positive non-small-cell lung cancer: is afatinib better or simply newer? J Clin Oncol 2013; 31: 3303–3306.
- Arcila ME et al. Rebiopsy of lung cancer patients with acquired resistance to EGFR inhibitors and enhanced detection of the T790M mutation using a locked nucleic acid-based assay. Clin Cancer Res 2011; 17: 1169–1180.
- Kuiper JL et al. Incidence of T790M mutation in (sequential) rebiopsies in EGFR-mutated NSCLC-patients. Lung Cancer 2014; 85: 19–24.
- Soria JC et al. Gefitinib plus chemotherapy versus placebo plus chemotherapy in EGFR-mutation-positive non-small-cell lung cancer after progression on first-line gefitinib (IMPRESS): a phase 3 randomised trial. Lancet Oncol 2015; 16: 990–998.
- Sharma SV et al. Epidermal growth factor receptor mutations in lung cancer. Nat Rev Cancer 2007; 7: 169–181.
- Maemondo M et al. Gefitinib or chemotherapy for non-small-cell lung cancer with mutated EGFR. N Engl J Med 2010; 362: 2380–2388.
- Mitsudomi T et al. Gefitinib versus cisplatin plus docetaxel in patients with non-small-cell lung cancer harbouring mutations of the epidermal growth factor receptor (WJTOG3405): an open label, randomised phase 3 trial. Lancet Oncol 2010; 11: 121–128.
- Fukuoka M et al. Biomarker analyses and final overall survival results from a phase III, randomised, open-label, first-line study of gefitinib versus carboplatin/paclitaxel in clinically selected patients with advanced non-small-cell lung cancer in Asia (IPASS). J Clin Oncol 2011; 29: 2866–2874.
- IRESSA EMA. Summary of Product Characteristics. Last updated October 2016. Accessed 26 January 2017.
- Yu HA, Arcila ME, Rekhtman N et al. Analysis of tumor specimens at the time of acquired resistance to EGFR-TKI therapy in 155 patients with EGFR-mutant lung cancers. Clin Cancer Res 2013; 19: 2240–2247.
- Cortot AB, Jänne PA. Molecular mechanisms of resistance in epidermal growth factor receptor-mutant lung adenocarcinomas. Eur Respir Rev 2014; 23: 356–366.
- Tagrisso FDA. Prescribing information. Last updated September 2016. Accessed 25 January 2017.
- Tagrisso summary of product characteristics. Last updated September 2016. Accessed 25 January 2017.
- cobas® EGFR Mutation Test v2 [package insert]. Indianapolis, IN: Roche Molecular Systems, Inc. 2016.
- Thress KS, Brant R, Carr TH, et al. EGFR mutation detection in ctDNA from NSCLC patient plasma: Across-platform comparison of leading technologies to support the clinical development of AZD9291. Lung Cancer 2015; 90: 509-515.
- Oxnard GR, Thress KS, Alden RS, et al. Association between plasma genotyping and outcomes of treatment with osimertinib (AZD9291) in advanced non–small-cell lung cancer. J Clin Oncol 2016; 34: 3375-3382.
A CONTINUACIÓN
Recoleccion de la muestra
Para realizar con éxito una prueba de mutación del receptor del factor de crecimiento epidérmico (EGFR), se requiere una cantidad suficiente de células tumorales para garantizar que se extraiga una cantidad adecuada de ADN tumoral para el análisis.
Conozca más
